Tyrosine
La tyrosine est un acide aminé aromatique, polaire.
Recherche sur Google Images :
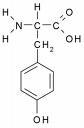
Source image : commons.wikimedia.org Cette image est un résultat de recherche de Google Image. Elle est peut-être réduite par rapport à l'originale et/ou protégée par des droits d'auteur. |
Définitions :
- (terme chimique; du gr. turos, fromage). Symbole Tyr. Acide aminé dérivé de la phénylalanine. Son rôle métabolique est particulièrement important... (source : nzdl.sadl.uleth)
- acide aminé précurseur de la dopamine, de la noradrénaline. (source : tpedepression.blogspot)
| Tyrosine | |
|---|---|
  |
|
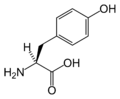
| Structure de la tyrosine | |
| Général | |
| Nom IUPAC | acide (S) -2-amino-3- (4-hydroxyphényl) propanoïque |
| Synonymes | Y, Tyr |
| No CAS | (racémique) (L) ou S (-) (D) ou R |
| No EINECS | |
| DrugBank | |
| PubChem | |
| ChEBI | |
| FEMA | |
| SMILES |
|
| InChI |
|
| Propriétés chimiques | |
| Formule brute | C9H11NO3 [Isomères] |
| Masse molaire | 181, 1885 g∙mol-1 C 59, 66 %, H 6, 12 %, N 7, 73 %, O 26, 49 %, |
| pKa | 2, 2 [1] |
| Propriétés physiques | |
| T° fusion | 343 °C (décomposition) [1] |
| Solubilité | 479 mg∙l-1 (eau, 25 °C) [1] |
| Thermochimie | |
| S0solide | 214, 01 J∙mol-1∙K-1 [2] |
| ΔfH0solide | -685, 6 kJ∙mol-1 [2] |
| Cp | 216, 44 J∙mol-1∙K-1 (solide, 25 °C) [2] |
| Précautions | |
|
|
|
| Produit non contrôlé | |
|
|
|
La tyrosine (Tyr ou Y) est un
Elle participe à la synthèse des catécholamines : l'adrénaline, la noradrénaline, la dopamine et la DOPA. Elle est aussi précurseur de la mélanine (pigment qui colore la peau, les poils, l'iris) et des hormones thyroïdiennes (formation de thyronine à partir de deux tyrosine).
Elle peut être synthétisée, dans le corps, à partir de la phénylalanine, sauf en cas de phénylcétonurie (maladie résultant d'une accumulation de phénylalanine dans le sang due à l'absence d'une protéine fonctionnelle : la phénylalanine hydroxylase). Elle est par conséquent non indispensable, sauf en l'absence de phénylalanine.
Le noyau aromatique de la tyrosine (ou parahydroxy phénylalanine) comprend un groupement hydroxyl qui rend sa chaine latérale moins hydrophobe que celle de la phénylalanine (mais la tyrosine est un acide aminé nettement moins soluble dans l'eau que la phénylalanine). Cette fonction hydroxyle lui permet d'être phosphorylée par des enzymes nommés kinases. La phosphorylation d'un acide aminé a fréquemment un rôle de régulation de l'activité de l'enzyme elle même. La thréonine et la sérine sont deux autres acides aminés pouvant subir la même phosphorylation.
La tyrosine peut aussi être modifiée en (3-) nitrotyrosine. Cette réaction de nitration peut affecter la tyrosine comme acide aminé libre ou que résidu d'acide aminé intégré dans une chaîne polypeptidique. In vivo, cette réaction est surtout due à l'action de l'acide péroxynitreux (ou péroxynitrite, ONOOH), mais d'autres voies réactionnelles peuvent aussi aboutir à la formation de nitrotyrosine. In vitro, le tétranitrométhane (TNM) a aussi été utilisé dans ce but. La nitration de tyrosines est le plus souvent vue comme un phénomène pathologique (e. g. l'augmentation de la concentration plasmatique de nitrotyrosine est reconnue comme un biomarqueur de phénomènes inflammatoires), quoique la possibilité que cette réaction soit aussi un phénomène physiologique ait récemment été suggérée.
Dans son assiette
De petites étoiles blanches sont visibles sur la tranche de section de certains fromage comme le Comté. Croquant sous la dent, des cristaux de tyrosine attestent de la protéolyse lors de la maturation. Cette tyrosine peu soluble dans l'eau se rassemble en fines cristallisations que savent apprécier les gourmets.
Liens externes
- http ://www. chups. jussieu. fr/polys/biochimie/STbioch/POLY. Chp. 11.19. html
- (en) http ://www. chemie. fu-berlin. de/chemistry/bio/aminoacid/tyrosin_en. html
Références
- (en) «Tyrosine» sur ChemIDplus, consulté le 8 juillet 2009
- (en) «Tyrosine» sur NIST/WebBook, consulté le 8 juillet 2009
- ↑ «Tyrosine (l-) » dans la base de données de produits chimiques Reptox de la CSST (organisme canadien responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
|
|
| Ala | Arg | Asn | Asp | Cys | Glu | Gln | Gly | His | Ile | Leu | Lys | Met | Phe | Pro | Ser | Thr | Trp | Tyr | Val |
| Acide aminé essentiel | Protéine | Peptide | Code génétique |
Recherche sur Amazone (livres) : |
Voir la liste des contributeurs.
La version présentée ici à été extraite depuis cette source le 05/11/2009.
Ce texte est disponible sous les termes de la licence de documentation libre GNU (GFDL).
La liste des définitions proposées en tête de page est une sélection parmi les résultats obtenus à l'aide de la commande "define:" de Google.
Cette page fait partie du projet Wikibis.



 Accueil
Accueil Recherche
Recherche Début page
Début page Contact
Contact Imprimer
Imprimer Accessibilité
Accessibilité